Οι ιογενείς αιμορραγικοί πυρετοί [Viral hemorrhagic fevers (VHFs)] έχουν παγκόσμια κατανομή, διατηρούνται μέσα από κύκλους μετάδοσης στο ζωικό βασίλειο, έχουν την τάση επέκτασης σε νέες γεωγραφικές περιοχές και σε νέα είδη ζώων. Ανήκουν στις οικογένειες Φλαβοϊών (Flaviviridae), Φιλοϊών ή Νηματοϊών (Filoviridae), Αρεναϊών (Arenaviridae), και Μπουνιαϊών (Bunyaviridae), υπάρχουν συχνά σε άγρια ή οικόσιτα ζώα, και κάποιοι από αυτούς προκαλούν αιμορραγικές εκδηλώσεις και βαριά κλινική εικόνα.
Τα κοινά χαρακτηριστικά των ιών αυτών περιλαμβάνουν τα παρακάτω στοιχεία:
- πρόκειται για RNA-ιούς με λιπιδικό περίβλημα,
- η επιβίωσή τους στο περιβάλλον εξαρτάται από ξενιστή (έντομο ή τρωκτικό, διαφορετικό για κάθε ιό),
- η γεωγραφική περιοχή κυκλοφορίας τους αντιστοιχεί στην περιοχή κυκλοφορίας του αντίστοιχου ξενιστή,
- ο άνθρωπος συνήθως μολύνεται όταν έρχεται σε επαφή με τον μολυσμένο ξενιστή των ιών αυτών, αλλά σε μερικές περιπτώσεις μετά την εκδήλωση της ασθένειας είναι δυνατή η μετάδοση της από άνθρωπο σε άνθρωπο.
- Σποραδικά εμφανίζονται ανθρώπινα κρούσματα αιμορραγικών πυρετών ή και επιδημίες χωρίς να είναι εύκολη η πρόβλεψή τους.
- Εκτός ελαχίστων εξαιρέσεων, τα νοσήματα που προκαλούν αυτοί οι ιοί δεν έχουν ειδική φαρμακευτική θεραπεία, παρά μόνο υποστηρικτική αγωγή.
Οικογένεια Flaviviridae (Φλαβοϊοί)
Δάγγειος πυρετός
Οι τέσσερις ορότυποι, 1-4, του ιού του Δάγγειου πυρετού (Dengue hemorrhagic fever viruses, DENVs), ανήκουν στην οικογένεια Flaviviridae (φλαβοϊοί), γένος flavivirus και υπάρχουν σε 100 χώρες τροπικών και υποτροπικών περιοχών. Η κλινική εικόνα ποικίλλει από αδιάγνωστη οξεία εμπύρετο νόσο και τυπικό Δάγγειο πυρετό έως τις απειλητικές για τη ζωή Δάγγειο αιμορραγικό πυρετό (Dengue hemorrhagic fever, DHF) και καταπληξία (Dengue Shock Syndrome, DSS). Ο ετήσιος αριθμός κρουσμάτων είναι πάνω από 100 εκατομμύρια λοιμώξεις, με 500.000 να αναπτύσσουν Δάγγειο αιμορραγικό πυρετό που μπορεί να εξελιχθεί σε καταπληξία, με θνητότητα 1-2.5% εάν ο ασθενής νοσηλευτεί ή έως 20% εάν ο ασθενής δεν νοσηλευτεί. Ο Δάγγειος μεταδίδεται με τα κουνούπια Aedes Aegypti και Aedes Albopictus. Ο αριθμός των κρουσμάτων αυξάνει τις τρεις τελευταίες δεκαετίες ως αποτέλεσμα της αποψίλωσης και αστικοποίησης ενδημικών περιοχών, σε συνδυασμό με τις φτωχές συνθήκες διαβίωσης, την έλλειψη ψεκασμών και επιτήρησης, των ανεπαρκών προγραμμάτων δημόσιας υγείας, των διεθνών ταξιδιών και της εξέλιξης του ιού και του διαβιβαστή του. Δεν υπάρχει εμβόλιο και η έρευνα απέχει ακόμη από τη δημιουργία του.
Μετάδοση με το Aedes Aegypti μπορεί να γίνει σε ευρύτατη περιοχή, στην οποία σύμφωνα με τον Παγκόσμιο Οργανισμό Υγείας περιλαμβάνεται και η Πορτογαλία, Ισπανία, και μερικώς και η Ελλάδα. Πράγματι, το 2012-2013 στη Μαδέρα της Πορτογαλίας εκδηλώθηκε επιδημία από τον ορότυπο 1, που πιθανώς εισήχθη από τη Ν.Αμερική με ταξιδιώτες μεταξύ της εβδομάδας 4 και 13 του 2013, μεταδόθηκε με το Aedes Aegypti που είναι γνωστό από το 2005 ότι έχει εγκατασταθεί στο νησί και προκάλεσε 2.168 πιθανά κρούσματα, εκ των οποίων τα 1080 επιβεβαιωμένα, χωρίς βαριά περιστατικά και χωρίς κανένα θάνατο. Αξίζει να σημειωθεί ότι μετάδοση έχει τεκμηριωθεί στην Κροατία και στη Γαλλία. Κρούσματα Δάγγειου έχουν εισαχθεί σε αρκετές ευρωπαϊκές χώρες με τουρίστες που επιστρέφουν από ενδημικές περιοχές όπως η Μαδέρα. Στο ΚΕΕΛΠΝΟ έχει δηλωθεί ένα κρούσμα Δάγγειου σε τουρίστα, ο οποίος επέστρεψε από την Ινδία.
Οικογένεια Filoviridae (Φιλοϊοί, Νηματοϊοί):
Η οικογένεια Filoviridae περιλαμβάνει τρία γένη, Ebolavirus (ebolavirus), Marburgvirus (marburgvirus) και Cuevavirus. Το γένος Ebolavirus διαιρείται σε πέντε είδη, Zaire ebolavirus (Ebola virus, EBOV), Sudan ebolavirus (Sudan virus, SUDV), Tai Forest ebolavirus (Tai Forest virus, TAFV), Bundibugyo ebolavirus (Bundibugyo virus, BDBV) και Reston ebolavirus (Reston virus, RESTV). Ο ιός Ebola Ebola έχει υψηλή λοιμογονικότητα για τον άνθρωπο. Είναι ιός RNA, ο οποίος με την εξαίρεση του Reston ebola virus προκαλεί σοβαρή νόσο με υψηλή θνητότητα που φθάνει το 88% στις ενδημικές περιοχές. Προέρχεται από τις νυχτερίδες. Απροστάτευτη επαφή με νεκρούς για οποιοδήποτε λόγο έχει ενοχοποιηθεί στη μετάδοσή του. Η αερογενής μετάδοση έχει μικρό αν όχι κανένα ρόλο για τους ανθρώπους, αν και έχει αποδειχθεί σε μαϊμούδες. Δεν υπάρχει κάποιο αποτελεσματικό αντιιϊκό για τον άνθρωπο και η ιντερφερόνη δεν ενδείκνυται. Χρειάζεται υποστηρικτική αγωγή του ασθενούς και αποφυγή παρεμβάσεων για να αποφευχθεί η αιμορραγία, με παράλληλη διατήρηση της ισοζυγίου υγρών και παρακολούθηση της πήξης.
Οικογένεια Arenaviridae (Αρεναϊοί)
Οι αρεναϊοί (arenaviruses) είναι RNA ιοί, τα υποδόχα τους είναι τρωκτικά, τα οποία μεταδίδουν τον ιό οριζόντια και κάθετα, έχουν χρόνια ιογενή λοίμωξη χωρίς εμφανή νόσο και μεταδίδουν τον ιό στους ανθρώπους με τα περιττώματά τους, κυρίως δε με τα ούρα τους. Σε αυτούς περιλαμβάνεται ο ιός Lassa, που υπάρχει σε τρωκτικά του παλαιού κόσμου, καθώς και οι ιοί Chapare και Machupo στη Βολιβία, Guanarito στη Βενεζουέλα, Junin στην Αργεντινή, Sabia στη Βραζιλία. Δεν υπάρχει εμβόλιο για κανέναν αρεναϊό. Η νόσος που προκαλεί ο ιός Lassa διαφέρει από άλλων αρεναϊών στο ότι μεταδίδεται από άτομο σε άτομο και έχει θνητότητα μεταξύ των νοσηλευόμενων 25% που στα παιδιά φτάνει στο 75%. Μεταδίδεται και με αερόλυμα και με άμεση επαφή με τρωκτικά, τα οποία ζουν στο χώρο κατοικίας ή με αερόλυμα σε εργαστήρια. Όσοι επιζούν έχουν κώφωση λόγω βλάβης του VIII νεύρου, σε ποσοστό 66% των νοσηλευομένων. Η ριβαβιρίνη μειώνει τη θνητότητα κατά 50%, όταν χορηγηθεί την πρώτη εβδομάδα της νόσου, και μετά την πρώτη εβδομάδα όσο πιο ενωρίς ληφθεί τόσο μειώνεται η θνητότητα. Απροφύλακτες επαφές με ασθενή με πυρετό Lassa χρειάζονται άμεση χορήγηση ριβαβιρίνης.
Oικογένεια Bunyaviridae:
Η οικογένεια Bunyaviridae περιλαμβάνει περισσότερους από 200 ιούς που υπάρχουν στο ζωικό βασίλειο και ταξινομούνται σε τέσσερα γένη: γένος Bunyavirus, Phlebovirus, Nairovirus και Hantavirus. Είναι ιοί RNA με μεγάλη ετερογένεια, παγκόσμια κατανομή, προσβάλλουν σπονδυλωτά, ασπόνδυλα και φυτά. Η γεωγραφική τους κατανομή και η δημιουργία των εστιών τους καθορίζονται από τη διατήρησή τους στη φύση μέσα σε κύκλους μετάδοσης σπονδυλωτών και των διαβιβαστών τους. Παράλληλα, επηρεάζονται από περιβαλλοντικούς παράγοντες και από κλιματολογικές συνθήκες. Κλινικά σημαντικοί ιοί είναι ο ιός του αιμορραγικού πυρετού της Κριμαίας Κογκό (Crimean Congo Hemorrhagic Fever Virus, CCHFV) του γένους Nairovirus και οι ιοί Hanta του γένους Hantavirus που προκαλούν βαριά κλινική εικόνα με αιμορραγικές εκδηλώσεις και θνητότητα από λιγότερο του 1% έως 60%. Παρατηρούνται σε ολοένα ευρύτερες περιοχές.
Ιός του αιμορραγικού πυρετού της Κριμαίας-Κογκό (Crimean-Congo Hemorrhagic Fever Virus, CCHFV):
Ο ιός του αιμορραγικού πυρετού της Κριμαίας-Κογκό (CCHFV) προκαλεί τη λοίμωξη αιμορραγικός πυρετός Κριμαίας Κογκό (Crimean-Congo Hemorrhagic Fever infection (CCHF infection), είναι κροτωγενής ιογενής ζωονόσος με τη δυνατότητα μετάδοσης από άνθρωπο σε άνθρωπο και ενδημεί σε μεγάλες περιοχές της Ασίας, Νοτιοανατολικής Ευρώπης και Αφρικής. Διατηρείται στη φύση σε κύκλους σπονδυλωτών και κροτώνων του γένους Ηyalomma, οι οποίοι είναι διαβιβαστές και δεξαμενή του ιού, καθώς μεταδίδουν τον ιό στα αυγά τους μολύνοντας την επόμενη γενεά τους. Η γεωγραφική κατανομή συμπίπτει με εκείνη του κρότωνα, σε μια ολοένα ευρύτερη γεωγραφική περιοχή που περιλαμβάνει πάνω από 30 χώρες, στην Αφρική, κεντρική και νοτιοανατολική Ασία, τη Μέση Ανατολή και τη Νοτιοανατολική Ευρώπη.
Στις ενδημικές περιοχές η λοίμωξη έχει καταδειχθεί με ανίχνευση ιού ή αντισωμάτων σε οικόσιτα σπονδυλωτά, όπως βοοειδή, αιγοπρόβατα, άλογα, χοίρους, στρουθοκάμηλους, καμήλες, σκύλους, αλλά και σκαντζόχοιρους, ποντίκια, λαγούς. Ερπετά και πτηνά με την εξαίρεση της στρουθοκαμήλου δείχνουν να είναι ανθεκτικά στη λοίμωξη. Επίσης, μεταναστευτικά πουλιά μεταφέρουν μολυσμένα τσιμπούρια σε νέες περιοχές, ενώ τα βοοειδή μεταφέρουν τσιμπούρια φορείς του ιού διαμέσου των συνόρων σε άλλη μη ενδημική χώρα. Ορολογικά δεδομένα δείχνουν ότι ο ιός υπάρχει χωρίς να προκαλεί νόσο στη Γαλλία, Πορτογαλία, Ουγγαρία, Αίγυπτο, και Ινδία, ενώ κρούσματα έχουν αναφερθεί από τις βαλκανικές χώρες. Το 2004 υπήρξε επιδημία στην Τουρκία, στην οποία δεκαετίες πριν υπήρχε ορολογική ανίχνευση του ιού.
Ο ιός CCHFV προκαλεί σοβαρή νόσο στον άνθρωπο και στα νεογέννητα ποντίκια. Η διάγνωση γίνεται με απομόνωση του ιού, με ορολογικές δοκιμασίες και με μοριακές τεχνικές. Η καλλιέργεια και η απομόνωσή του γίνονται μόνο σε εργαστήριο με υψηλό επίπεδο βιοασφάλειας. Τα αντισώματα ανιχνεύονται με ELISA 7 – 14 μέρες μετά την έναρξη συμπτωμάτων, αλλά δεν ανιχνεύονται, όταν ο θάνατος έχει συμβεί εντός τεσσάρων ημερών από την έναρξη συμπτωμάτων. Η αλυσιδωτή αντίδραση πολυμεράσης με ανάστροφη μεταγραφάση (RT-PCR) θέτει τη διάγνωση σε αυτή την περίπτωση.
Ο άνθρωπος μολύνεται με άμεση επαφή με αίμα και ιστούς ξενιστών με ιαιμία ή με δήγμα μολυσμένου κρότωνα ή με σύνθλιψη κρότωνα με απροστάτευτα χέρια. Στις ενδημικές περιοχές ομάδες υψηλού κινδύνου είναι εκείνοι που έχουν αγροκτηνοτροφικές ασχολίες ή περνούν τον ελεύθερο χρόνο τους σε περιοχή με κρότωνες χωρίς προστασία. Ογδόντα τοις εκατό των λοιμώξεων είναι ασυμπτωματικές. Η δεύτερη ομάδα κινδύνου στις ενδημικές περιοχές είναι οι εργαζόμενοι στο χώρο της υγείας ως αποτέλεσμα των παρεμβάσεων σε ασθενείς με CCHFV λοίμωξη και σηματοδοτούν την ύπαρξη επιδημίας στην κοινότητα. Η θνητότητα είναι από 10% έως 50%, όταν η μετάδοση γίνεται σε νοσοκομειακό περιβάλλον, ενώ εκτιμάται ότι είναι μικρότερη όταν γίνεται στην κοινότητα. Η ριβαβιρίνη είναι φάρμακο εκλογής μαζί με υποστηρικτική αγωγή. Κλιματολογικές και περιβαλλοντικές μεταβολές ενδέχεται να επηρεάσουν τη γεωγραφική κατανομή και να προκαλέσουν επιδημίες.
Στην Ελλάδα, οροεπιδημιολογικές μελέτες ανέδειξαν την παρουσία λοίμωξης σε ανθρώπους χωρίς ιστορικό σοβαρής νόσου και μάλιστα η συχνότητα ανίχνευσης CCHF IgG αντισωμάτων σε ορισμένες περιοχές (ημιορεινή Θεσπρωτία) φτάνει το 14,4% χωρίς και πάλι να έχουν αναφερθεί κρούσματα. Οι αγροκτηνοτροφικές δραστηριότητες και η σφαγή είχαν 4.17 και 2.69 φορές μεγαλύτερο κίνδυνο επαφής με τον ιό. Η απουσία κρουσμάτων ίσως υποκρύπτει λοίμωξη από τον χαμηλής παθογονικότητας ιό ΑΡ92. Παράλληλα, η οροθετικότητα σε αυτή τη μοναδική κατάσταση στην Ελλάδα ίσως παρέχει προστασία στον πληθυσμό. Στην Ελλάδα έχει καταγραφεί μόνο ένα κρούσμα, το οποίο απεβίωσε, ήταν κοντά στα βορειοανατολικά σύνορα της χώρας μας το 2008. Ο ιός ήταν διαφορετικός από τον ΑΡ92 και όμοιος με εκείνον των Βαλκανίων, της Ρωσίας και της Τουρκίας. Στην ίδια περιοχή ο επιπολασμός αντισωμάτων έχει αυξηθεί σημαντικά, πιθανώς λόγω μεταβολής στο κλίμα είτε μετακίνησης (νόμιμης ή παράνομης) ζώων ή πτηνών με κρότωνες που φέρουν τον ιό.
Ιοί Hanta:
 Η δομή του ιού Hanta Οι Hanta ιοί είναι:
Η δομή του ιού Hanta Οι Hanta ιοί είναι:
- Ο Sin Nombre virus (SNV) που υπάρχει στην Αμερικανική Ήπειρο και προκαλεί πνευμονικό σύνδρομο από Hanta ιό (hantavirus pulmonary/cardiopulmonary syndrome, HPS) με θνητότητα 60%. Υποδόχο του ιού είναι το τρωκτικό deer mouse Peromyscus maniculatus, που είναι ευρέως διαδεδομένο στην Αμερικανική Ήπειρο, και διαβιεί εντός κατοικιών και άλλων εγκαταστάσεων.
- Ο Hantaan Virus (HTNV) προκαλεί Hemorrhagic fever with renal syndrome (HFRS) στην Κορέα, την Κίνα και την Ανατολική Ρωσία, με δεξαμενή (υποδόχο) το ποντίκι του αγρού, Apodemus agrarius. Ζει σε αγροτικές περιοχές ή κοντά σε αυτές, και προκαλεί αυξημένη συχνότητα της νόσου την άνοιξη και το φθινόπωρο. Προκαλεί κλινική εικόνα βαρέως πάσχοντος με θνητότητα 5%.
- Ο Seoul virus (SEOV) με ευρύτατη γεωγραφική κατανομή όπως ακριβώς και δεξαμενή του ο αρουραίος Rattus Norvegicus, αλλά στην Ασία προκαλεί ηπιότερη κλινική εικόνα σε σύγκριση με εκείνη του HTNV. Η επαφή με το τρωκτικό μπορεί να συμβεί στον αγρό αλλά και εντός αστικών περιοχών όπως έχει τεκμηριωθεί για παράδειγμα για την Σεούλ.
- Ο Dobrava-Belgrade (DOBV).
- Ο Puumala (PUUV) που ενδημούν στην Ευρώπη και προκαλούν στην Ασία και την Ευρώπη αιμορραγικό πυρετό και νεφρωσικό σύνδρομο (Hemorrhagic Fever Renal Syndrome, HFRS) με θνητότητα που κυμαίνεται από <1% έως 12%.
Η διάθεση μοριακών τεχνικών δίνει πληροφορίες για το γενετικό υλικό και θέτει οριστική διάγνωση για όλους τους ιούς και για τους γονότυπους του ιού Dobrava-Belgrade (DOBV) και βοήθησαν στην κατάταξη και ονοματολογία τους. Παρόλα αυτά οι περισσότεροι ασθενείς διαγιγνώσκονται με ορολογικές τεχνικές, οι οποίες ανιχνεύουν ειδικά αντισώματα έναντι του ιού Dobrava-Belgrade και Puumala, χωρίς να διαχωρίζουν ανάμεσα στους επιμέρους γονότυπους αυτών. Αυτό εξηγεί γιατί έχουν ανιχνευτεί αντισώματα για την παρουσία των ιών Hanta στην Ελλάδα ήδη από το 1981, αλλά και στις χώρες της Πρώην Γιουγκοσλαβίας με πολυάριθμα κρούσματα και επιδημίες, στην Αλβανία, Βουλγαρία, Σλοβακία, Γερμανία, Εσθονία, και Ρωσία. Αξίζει να σημειωθεί ότι αυξάνει ο αριθμός των χωρών, στις οποίες ανιχνεύονται αντισώματα στα τρωκτικά, ενώ στην Αμερική, Ασία, και Σκανδιναβία και σε όλες τις ενδημικές περιοχές αυξάνει ο αριθμός των κρουσμάτων. Εκτιμάται ότι κάθε χρόνο προσβάλλονται από τη νόσο 150.000 έως 200.000 άνθρωποι, εκ των οποίων το 70%-90% συμβαίνει στην Κίνα.
Οι Hanta ιοί μεταδίδονται με αερόλυμα ξηρών απεκκρίσεων (κόπρανα, ούρα, σίελος) κατά τη διάρκεια μακρών χρονικών περιόδων από τρωκτικά της οικογένειας Muridae τα οποία έχουν χρόνια λανθάνουσα λοίμωξη. Είδη ποντικού (shrews), τυφλοπόντικες και νυχτερίδες είναι και αυτά δεξαμενές που δεν έχουν μελετηθεί επαρκώς. Διάφορα τρωκτικά ενδέχεται να έχουν αντισώματα ή αντιγόνα διαφόρων Hanta ιών, αλλά κάθε είδος είναι δεξαμενή ενός κυρίως ιού. Η σταθερή συχνότητα κάθε ιού σε κάθε υποδόχο οφείλεται και στην οριζόντια μετάδοση μεταξύ σεξουαλικώς ενεργών τρωκτικών.
Οι Hanta ιοί Dobrava-Belgrade και Puumala στην Ευρώπη και τα Βαλκάνια:
Ο ιός Dobrava-Belgrade (DOBV) έχει ως δεξαμενή το ποντίκι Αpodemus flavicollis και αποτελεί το κύριο αίτιο της βαριάς κλινικής μορφής της νόσου που έχει θνητότητα 10% στα Βαλκάνια και 12% στις άλλες περιοχές. Δεύτερος σε συχνότητα που ενδημεί στη Σκανδιναβία, τη Δυτική Ρωσία και τη Βόρειο Ευρώπη, είναι ο ιός Puumala (PUUV) που έχει ως δεξαμενή του τον ποντικό Clethrionomys glareolus και αποτελεί το κύριο αίτιο της ήπιας μορφής της νόσου η οποία ονομάζεται επιδημική νεφροπάθεια (nephropathia epidemica) με θνησιμότητα <1%.
Και τα δυο είδη τρωκτικών ζουν στα δάση, πηγαίνουν σε αγροτικές εκτάσεις και ημιαστικούς κήπους και οικισμούς ιδιαίτερα τα έτη που ο πληθυσμός τους εμφανίζει αύξηση, και προκαλούν αυξημένη επίπτωση της νόσου στον άνθρωπο. Επισκέπτες ή εργάτες στα δάση και στα αγροκτήματα, βοσκοί, και στρατιώτες ενδέχεται να έλθουν σε επαφή με τον Apodemus ή τον Clethrionomys.
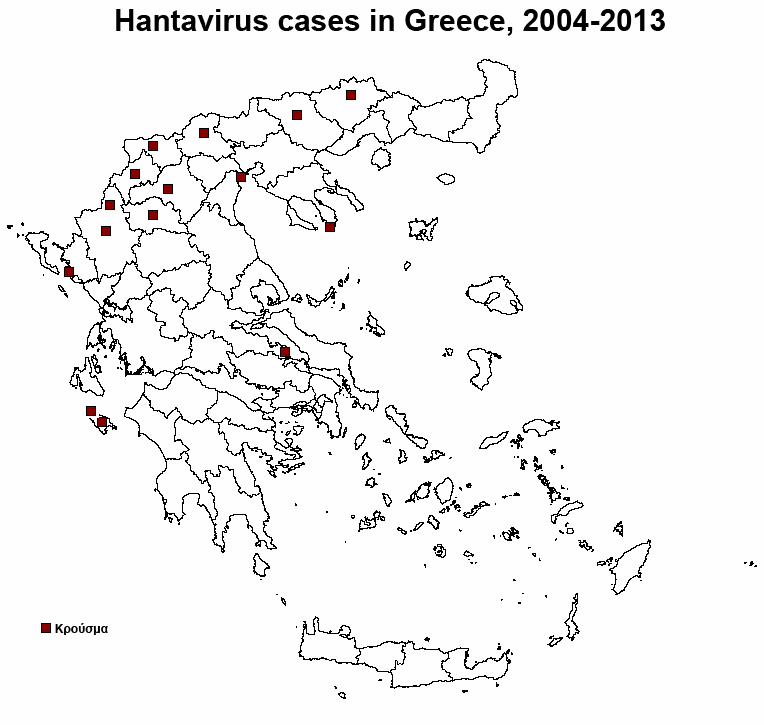 Γεωγραφική κατανομή κρουσμάτων HFRS στην Ελλάδα, 2004-2013
Γεωγραφική κατανομή κρουσμάτων HFRS στην Ελλάδα, 2004-2013
Ο ιός Dobrava-Belgrade περιγράφηκε για πρώτη φορά το 1992, όταν δυο αναφορές από την πρώην Γιουγκοσλαβία περιέγραψαν την απομόνωση ενός Hanta ιού, ο οποίος κυκλοφορούσε στα Βαλκάνια για πρώτη φορά. Ο ιός Belgrade απομονώθηκε από το αίμα και τα ούρα βαρέως πάσχοντος με οξύ αιμορραγικό πυρετό με νεφρικό σύνδρομο (ΗFRS), ενώ ο άλλος με το όνομα Dobrava, απομονώθηκε από τους πνεύμονες του Apodemus flavicollis (yellow necked mouse) στο χωριό Dobrava της Σλοβενία. Οι δυο ιοί είναι φυλογενετικά σχεδόν ίδιοι και η διεθνής επιτροπή για την ταξινόμηση των ιών πρότεινε το όνομα Dobrava-Belgrade (DOBV). Ο ιός DOBV έχει προκαλέσει χιλιάδες κρούσματα στα Βαλκάνια. Στην Ελλάδα σχεδόν όλα τα κρούσματα οξέος αιμορραγικού πυρετού με νεφρικό σύνδρομο (HFRS) προκαλούνται από τον ιό DOBV.
Παρόλα αυτά η αναλογία DOBV προς PUUV μειώνεται σταδιακά από 50% στη Νοτιοανατολική Ευρώπη σε λιγότερο από 1% στη Βορειοδυτική Ευρώπη, τη Σκανδιναβία και τις παρακείμενες περιοχές της πρώην Σοβιετικής ένωσης όπου ο ιός PUUV επικρατεί.
Ο ιός Dobrava-Belgrade δείχνει εποχιακή κατανομή με μεγαλύτερη επίπτωση το καλοκαίρι. Η αναλογία φύλου είναι τρεις άνδρες προς μία γυναίκα και η πλέον επηρεαζόμενη ηλικιακή ομάδα είναι των 35-40 ετών. Μετάδοση από άνθρωπο σε άνθρωπο δεν έχει αναφερθεί, ενώ η επίπτωση της νόσου δεν είναι γνωστή ιδιαίτερα μάλιστα για την επιδημική νεφροπάθεια που αποτελεί την ήπια κλινική εικόνα της νόσου.
Το 1981 ορολογική έρευνα στην Ελλάδα έδειξε ότι ένας Hanta ιός ενδημεί, το 1984 διαγνώστηκε ορολογικά για πρώτη φορά η νόσος που προκαλεί ο ιός και το 1989, με μελέτη 27 ορολογικά διαγνωσθέντων βαριάς μορφής περιστατικών, περιγράφηκαν τα κλινικά και εργαστηριακά χαρακτηριστικά της νόσου που ενδημεί στη χώρα μας.
Το 1996 το RNA του Dobrava-Belgrade ανιχνεύτηκε στο αίμα ενός Έλληνα και ενός Αλβανού ασθενούς με σοβαρό οξύ αιμορραγικό πυρετό με νεφρικό σύνδρομο (HFRS) καθώς και από τα Apodemus flavicolis που εντοπίστηκαν το 2000 στην περιοχή κατοικίας του Έλληνα ασθενούς. Οι πλέον ενδημικές περιοχές για τον ιό DOBV είναι η βορειοανατολική και η βορειοδυτική άκρη της Ελλάδας κατά μήκος της οροσειράς της Πίνδου και της Ροδόπης. Στην Ελλάδα εισάγονται ετησίως για νοσηλεία για τη νόσο 5 περίπου κρούσματα. Από το 2004 και μετά στο ΚΕΕΛΠΝΟ έχουν δηλωθεί δεκαοκτώ ασθενείς, εκ των οποίων οι δώδεκα ήταν Ελληνικής υπηκοότητας και οι έξι ήταν αλλοδαποί, εκ των οποίων οι δώδεκα ζούσαν σε νομούς της Βορείου Ελλάδος.
Όπως φαίνεται ο ιός είναι ενδημικός στη Βόρειο Ελλάδα, συνεπώς οι κλινικοί ιατροί πρέπει να εντάσσουν το νόσημα στη διαφορική τους διάγνωση ιδιαίτερα σε ασθενείς των ομάδων υψηλού κινδύνου με πυρετό, θρομβοπενία, ή σημεία νεφρικής βλάβης.
Στην Ελλάδα και τις γειτονικές της Βαλκανικές χώρες είναι εμφανές ότι οι Hanta ιοί και ο ιός CCHFV ενδημούν και οροεπιδημιολογικές μελέτες δείχνουν αυξανόμενο επιπολασμό αντισωμάτων έναντι των ιών αυτών, οι οποίοι μπορούν δυνητικά να επεκταθούν γεωγραφικά ή να αποκτήσουν μεγαλύτερη επίπτωση, ως αποτέλεσμα των κλιματικών συνθηκών. Για τους Hanta ιούς η γεωγραφική επέκταση υπάρχει σε όλες τις ηπείρους.
Ο κίνδυνος να μεταδοθούν οι πυρετοί Lassa, Marburg and Ebola είναι πολύ χαμηλός σε αντίθεση με τη λοίμωξη από Hanta ιούς που είναι συχνή σε ταξιδιώτες. Ωστόσο η διασπορά και μετάδοση της λοίμωξης από ιό Lassa σε εργαστήρια και σε κατοικίες με τρωκτικά στις ενδημικές περιοχές της Δυτικής Αφρικής και η λοίμωξη με ιό Marburg διαφόρων πιθηκοειδών που εισέπνευσαν σκόνη από περιττώματα νυχτερίδων, δείχνουν τον πιθανό κίνδυνο για τους τουρίστες στις ενδημικές περιοχές. Δεν έχει αναφερθεί ποτέ μετάδοση σε συνταξιδιώτη και μόνο μια ασυμπτωματική ορομετατροπή συνέβη σε 2000 επαφές στα νοσοκομεία των Δυτικών χωρών. Αντίθετα η μετάδοση σε επαγγελματίες υγείας αποτελεί πρόβλημα στις ενδημικές περιοχές.
Πηγή: Ενημερωτικό δελτίο ΚΕΕΛΠΝΟ - Απρίλιος 2014